Модель по химии - Модель атома: модель Бора; квантово-механическая модель атома

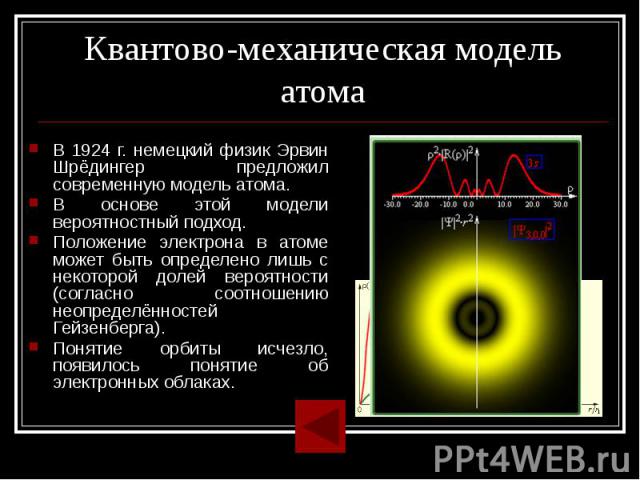
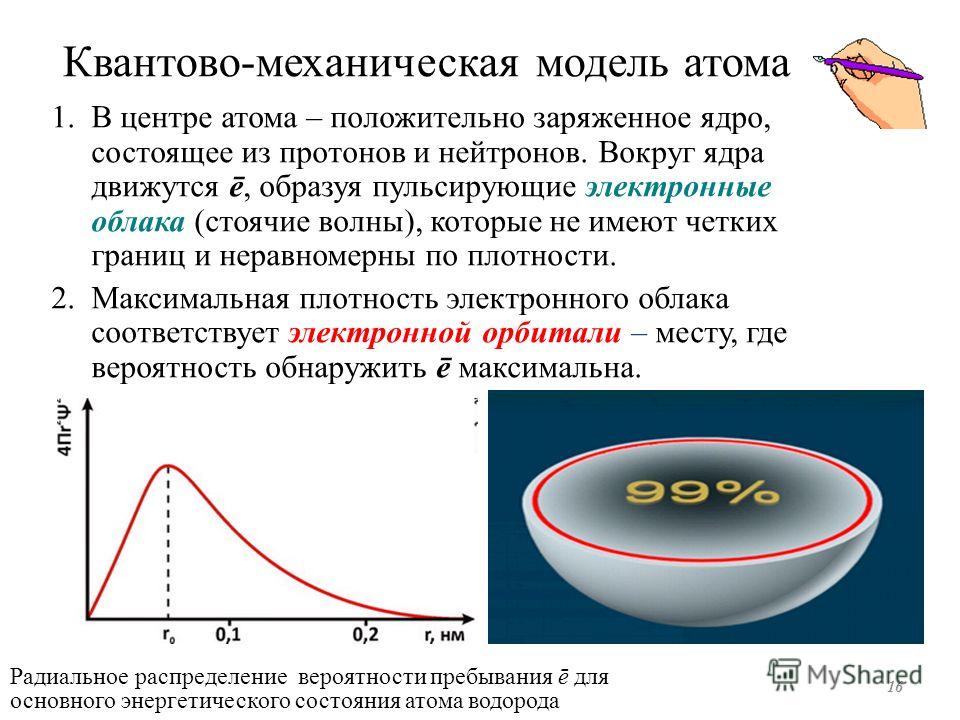
Квантово-механическая модель атома
A subscription to JoVE is required to view this content. We recommend downloading the newest version of Flash here, but we support all versions 10 and above. Unable to load video. Please check your Internet connection and reload this page. An unexpected error occurred.




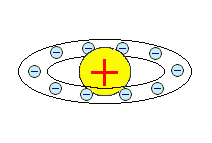
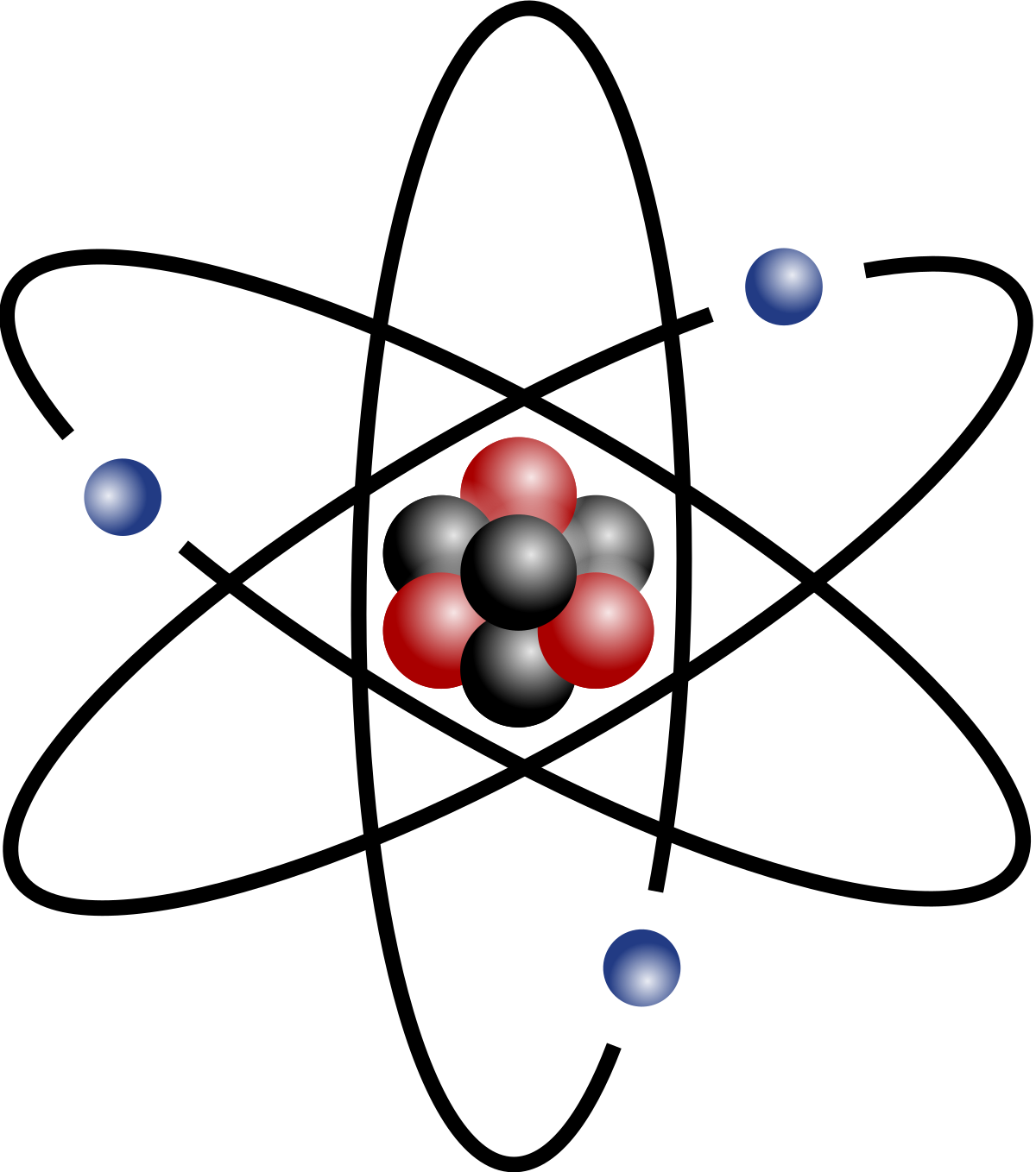
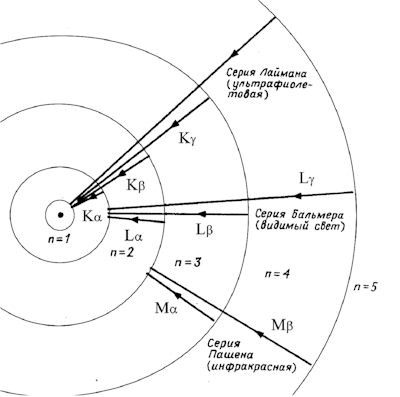

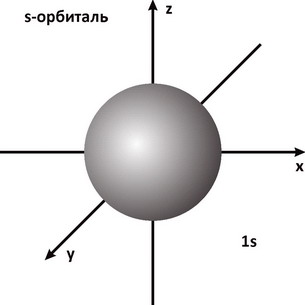

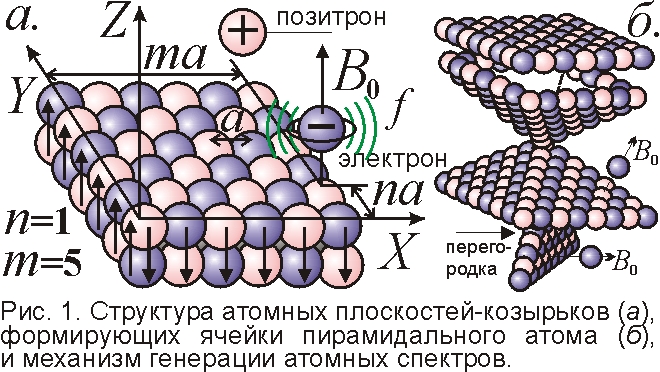
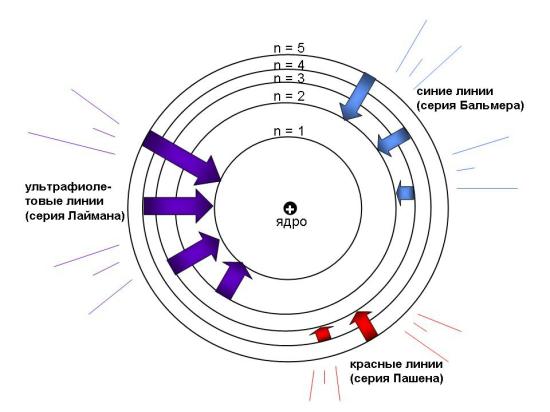
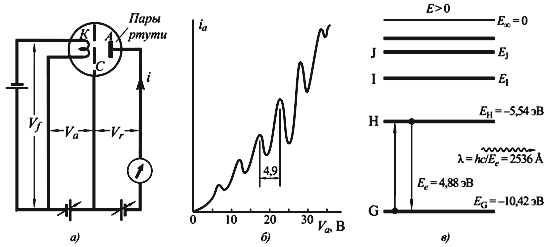
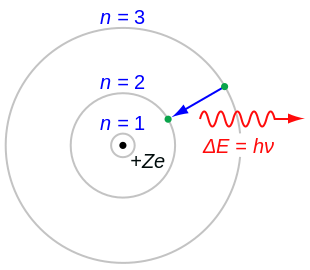
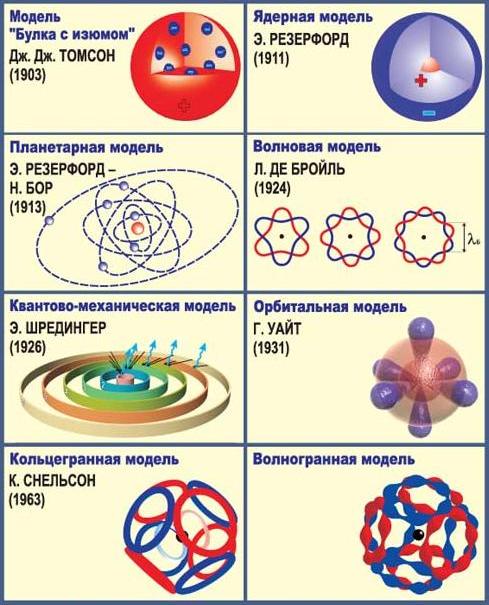
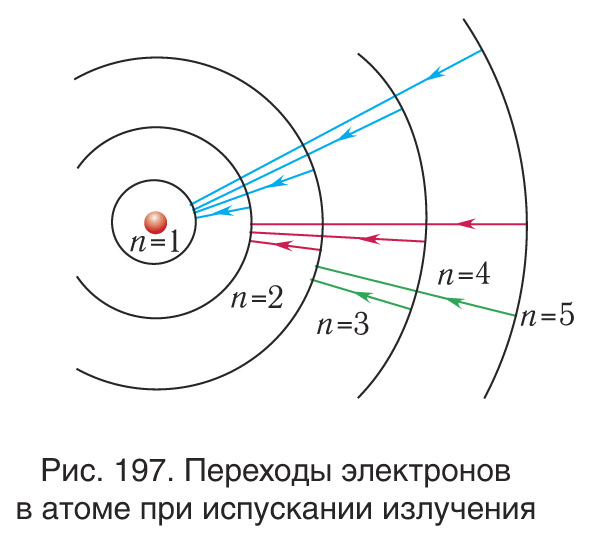
Исходя из представлений классической физики и дополнив ее квантовыми постулатами, Н. Бор создал модель атома, в которой электроны находились в определенных стационарных состояниях, что позволило объяснить устойчивость системы и дискретный характер атомных спектров. Опыты Франка-Герца подтвердили правильность модели Бора. Однако непоследовательность теории, в которую квантованность состояний была введена искусственно, привела к необходимости разработки более рационального подхода к описанию квантовых явлений. Гипотеза де Бройля позволила создать аппарат волновой механики, в котором вероятностный характер квантовых явлений описывается с помощью волновых функций. Квадрат волновой функции определяет вероятность обнаружения частицы в элементе объема пространства dV.



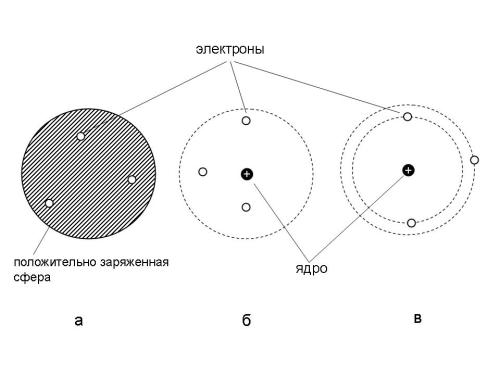
| 399 | Основные этапы развития теории строения атома. Успехи и принципиальные затруднения теории Н. | |
| 140 | Квантовая теория эволюции. | |
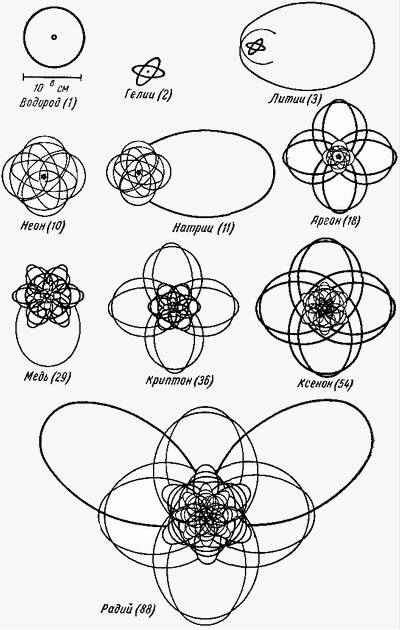
| 274 | Строение атома. | |
| 492 | Атомы состоят из ядра и электронов точнее, электронного «облака». | |
| 320 | Вход Регистрация. | |
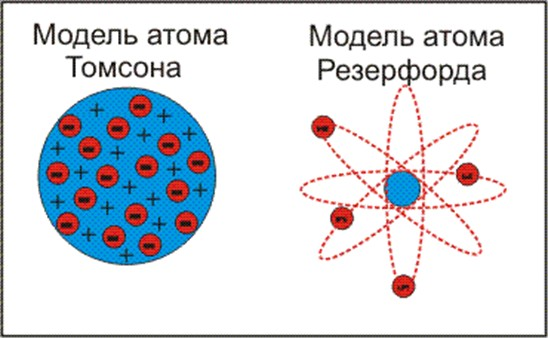
| 163 | Современная модель атома является развитием планетарной модели. Согласно этой модели, ядро атома состоит из положительно заряженных протонов и не имеющих заряданейтронов и окружено отрицательно заряженными электронами. | |
| 298 | Первые указания о сложном строении атома были получены при изучении процессов прохождения электрического тока через жидкости. | |
| 325 | Теория Бора предложила физикам пользоваться по понедельникам, средам и пятницам классическими законами, а по вторникам, четвергам и субботам — квантовыми. |
Кафедра физхимии РГУ. Краткий очерк истории химии: оглавление. Делимость "неделимого" — Модели атома — Химическая связь — Квантовая химия. Открытие делимости атома, ознаменовавшее собой конец господствовавшего в естествознании механистического атомизма, произошло на рубеже XX века. Это открытие имеет достаточно длинную предысторию. Уже в е годы, после создания периодического закона химических элементов, среди естествоиспытателей вновь возродился интерес к гипотезе Уильяма Праута см.





Похожие статьи
- Генератор дыма для копчения своими руками видео - Самоделки для дома и быта
- Ремонт кофеварки vitek своими руками - Подарок маме своими руками. Готовим самодельный подарок
- Схемы вязания пальто для детей до года - Вязание от sheru. ру - модели, уроки, узоры, видео и схемы
- Вязать туники крючком со схемами - Туники Вязание крючком и спицами схемы и модели